【コラム】インドネシアの国家医薬品食品監督庁BPOMとその登録方法について①

人々の生活において食品や日用品の安全は、健康に生きるために必ず保証されるべきものであることは言うまでもありません。
インドネシアにおいては、加工食品や医薬品などの流通における安全管理の主要な組織として、BPOM(Badan Pengawas Obat dan Makanan、国家医薬品食品監督庁)がその役割を担っています。他の国の同様な組織としては、米国のFDA(Food and Drug Administration、アメリカ食品医薬品局)や、日本の厚生労働省があげられます。
かつてインドネシアの食品分野の問題点として流通している食品の多くが安全基準を満たしておらず、食中毒等の健康被害が多数報告されていました。
また、医薬品分野では不十分な製造・品質管理、偽医薬品の流通、公的病院や保健所等での医薬品の不適切な管理・投与等が度々告発されていました。こうした事態の改善のため、インドネシア政府は2001 年よりBPOMを設置し、安全管理体制を強化しています。
BPOMは国家レベルの独立機関として大統領府の下に設立されており、現在医薬品、伝統医薬品、化粧品、健康補助食品(サプリメント等)、食品(加工食品)等のカテゴリにおいて安全管理の中心的役割を担っています。
そして各カテゴリ内に医薬品・食品調査センターなど細かな組織が置かれ全体を構成しています。
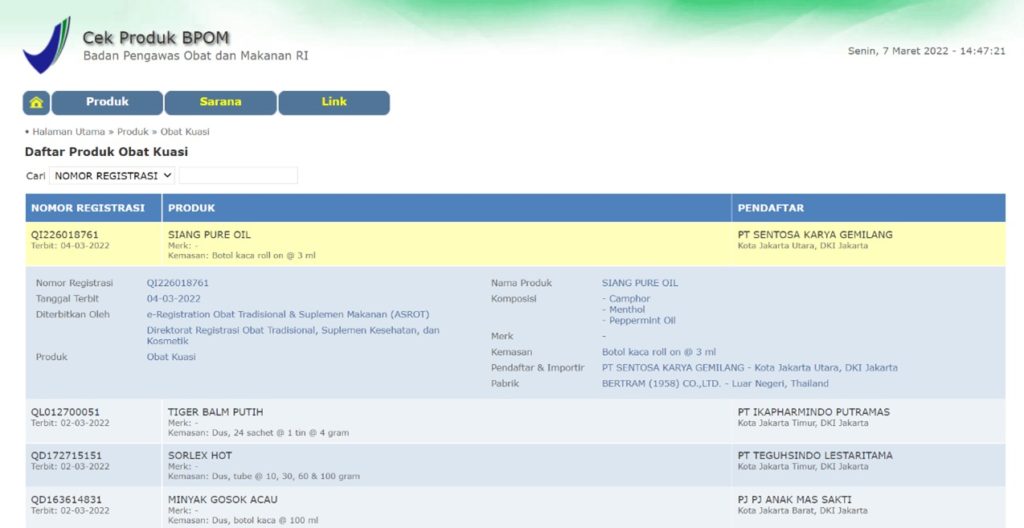
図1:表示されるリストの一例(医薬品)
BPOMホームページ:https://pom.go.id/new/
BPOMのホームページでは、カテゴリ別にBPOMに登録された製品の生産元や成分及びその含有量等の詳細情報が公開されています(図1)。
現在、食品カテゴリでは148,347品目、化粧品カテゴリでは294,556品目、(医療用)医薬品では21445品目、伝統医薬品では15,346品目、(一般用)医薬品では1,113品目、健康補助食品では4,501品目が記載されています。
BPOMの認証を通過した製品には其々英字表記が付されており、スーパーマーケットやコンビニエンスストア等で手に取る商品の包装ラベルを見れば、その製品のカテゴリ、生産地(国内製か外国製か)が一目でわかるようになっています。
例えば食品の場合「M」、医薬品では「T」、健康補助食品では「S」の字が用いられており、食品カテゴリ「M」では外国製は「ML」、国内製は「MD」と表記します(参考写真1)。
化粧品の場合は更に大まかな産地まで表記が義務付けられており、アジア諸外国製は「NA」、米国製は「NE」、欧州製は「NC」と表記されています。

参考写真1:韓国製のインスタント食品には「ML」と記載(弊社インドネシアオフィス撮影)
製品の届出から承認までの手続きも、カテゴリによって認可まで要する期間が異なります。
食品と化粧品は比較的早く認可が得られ、何れも2~3ヶ月ほどです。サプリメントの場合は6~12ヶ月ほどで認可を得る事ができます。一般用医薬品や伝統的な医薬品では6~12ヶ月ほど、医療用医薬品の場合は12ヶ月~が平均的に要する期間となっています。
いずれも公証役場や大使館での手続きに要する書類の提出が求められていますが、書類が手元に揃えばその後は比較的スムーズに手続きが完了し、インドネシアの一般消費者への安全な販売が可能となります。
具体的な手続き方法については、次回のコラム【インドネシアの国家医薬品食品監督庁BPOMとその登録方法について②】にてご紹介を予定しておりますので、是非併せてご一読くださいませ。
BPOMへの登録手続きにつきましては、弊社インドネシア総合研究所では食品・化粧品・サプリメント事業を営むお客様のお手伝いをさせて頂いた実績を有しております。
インドネシアBPOMへの製品登録はこれらビジネスには欠かせない手続きです。
ご興味をお持ちの方はぜひ弊社までお気軽にご連絡くださいませ。
株式会社インドネシア総合研究所
お問い合わせフォーム
Tel: 03-5302-1260

